الصناعة تواجه مخاوف جديدة بشأن سلامة الأدوية القديمة
ترجمة :عدنان الحاجي
تقديم د. غسان بوخمسين
الصناعة تواجه مخاوف جديدة بشأن السلامة من الأدوية القديمة والفحوصات الأوسع نطاقًا التي ستجرى عليها في ٢٠٢٠
المقدمة:
معلومات مهمة عن قضية تلوث بعض الأدوية بالمواد المسرطنة التي تكرر انتشارها مؤخراً
ثنائي ميثيل النتروسوأمين NDMA-Nitrosodimethylamine (1) مادة كيميائية شبه متطايرة، تتواجد طبيعياً في نبات التبغ، وقد تُنتج صناعياً بشكل ثانوي في بعض المنظفات والمذيبات والأصباغ، وقد تتسرب لمياه الشرب عرضياً عن طريق معالجة المياه بالكلوروأمين من أجل التعقيم ، وقد توجد هذه المادة بمستويات منخفضة جدًا في اللحوم المطبوخة أو المدخنة أو المعالجة، التي يُستخدم فيها مادة نيترات الصوديوم sodium nitrite كمادة حافظة، لذلك صُنفت هذه اللحوم مؤخراً كمواد مسرطنة محتملة.
هذه المادة صفراء اللون لا طعم ولا رائحة لها وقابلة للذوبان في الماء. تعتبر هذه المادة سامة للكبد والأجهزة الأخرى، وهي مادة مسرطنة محتملة للإنسان. كما أنها قد تستخدم لإستحداث سرطان في الفئران لأغراض بحثية.
صُنفت هذه المادة حسب المنظمة الدولية لأبحاث السرطان International Agency for Research on Cancer IRAC الذراع الرسمي التابع لمنظمة الصحة العالمية WHO كمادة مسرطنة محتملة من المجموعة الثانية (أي أنها مادة مسرطنة محتملة بشكل قوي لكن غير حاسم) في البشر. هذا التصنيف يعني:
١- وجود دراسات كثيرة وصارمة على الحيوانات تثبت تسبب هذه المادة للسرطان.
٢- أدلة محدودة على تسبب هذه المادة للسرطان على البشر.
٣-وجود أدلة قوية على أن للمادة خصائص مهمة في زيادة احتمالية تسبيب السرطان.
آلية التسبب في التسرطن لهذه المادة تُعزى إلى تسببها في طفرات جينية في الحمض النووي DNA مما يؤدي إلى خلل وأضرار فيه غير قابلة للإصلاح مما قد ينتج عنه سرطان في الكبد على وجه الخصوص .
برزت هذه المادة كثيراً في الإعلام في السنتين الأخيرتين، نتيجة لتكرار إعلان هيئة الغذاء والدواء الأمريكية FDA عن تلوث بعض الأدوية بهذه المادة بشكل عرضي، مما قد يشكل خطراً على الصحة ولذا أصدرت أمراً بسحب تلك الأدوية من الأسواق، حيث أُعلن عن تلوث دواء ڤالسارتن valsartan بهذه المادة وسُحب عام ٢٠١٨، وحصل نفس الأمر لدواء رانيتيداين ranitidine وسُحب من الأسواق عام ٢٠١٩. حسب ال FDA فأن المستوى المسموح به للتعرض لهذه المادة هو حوالي 96 نانوغرام nanogram (1000 نانوغرام = مايكروغرام) تقريباً في اليوم.
يُعزى سبب تواجد هذه المادة المسرطنة في الأدوية إلى تلوث المواد غير الفعالة ، التي تضاف إلى المادة الفعالة في الدواء، بهذه المادة بشكل عرضي، وذلك بسبب سوء التصنيع وعدم الاهتمام الكافي بطرق التصنيع الجيد GMP، وهذا يُلقي بتبعة إضافية على المصانع بالاهتمام أكثر بطرق التصنيع لضمان عدم التلوث بمثل هذه المواد، والحرص على استيراد المواد الداخلة في تصنيع الأدوية سواء المادة الفعالة أو المواد المضافة من مصادر موثوقة تهتم بالجودة في الصناعة. ومن الجدير بالذكر، لقد كشفت بعض التقارير أن معظم تلوث الأدوية بهذه المادة صادر من مصانع في الهند والصين، حيث تتميز منتجات تلك المصانع برخص الثمن وعدم الاهتمام بالجودة.
قد يبرز هنا كتساؤل مهم، لماذا برزت هذه المشكلة في الفترة الأخيرة فقط ولم نسمع بها من قبل، والجواب على هذا التساؤل هو للتحسن الكبير الذي حصل على طرق الكشف على هذه المادة ولو كانت بتراكيز ضئيلة جداً أكثر من ذي قبل، حيث لم يكن ذلك متاحاً حتى وقت قريب، كذلك زيادة الوعي لدى السلطات الصحية بأهمية الكشف عن هذه المادة وحماية المرضى من التعرض لها. وهذا من الأمثلة الممتازة لما يعرف بالتيقظ الدوائي Pharmacovigilance وهو الجانب الصيدلاني الذي يُعنى بالجمع والكشف والتقييم والرصد للمعلومات الدوائية، من أجل الوقاية من الآثار الضارة الناتجة عن المنتجات الصيدلانية.
لا تُخفي السلطات الصحية حول العالم مخاوفها المتزايدة من تكرار المشكلة في المستقبل بسبب استمرار وجود أسبابها، مما قد يكون سبباً لأزمتين في وقت واحد: الأولى تكمن في حصول نقص في توفر الأدوية ومعاناة المرضى من جراء ذلك وما يعني ذلك من مشاكل صحية واقتصادية على حد سواء، والثانية اختلال في ثقة المستهلك في جودة وسلامة الأدوية من المصانع وربما يتسبب ذلك في امتناعه عن تناولها وهذا أمر خطير قد يهدد صحة المرضى .
أشارت تقارير عدة قبل شهرين في أمريكا عن احتمالية تلوث أدوية كالميتفورمين المعروف لعلاج مرض السكري metformin ب NDMA وقد سُحب من أسواق بعض الدول مثل سنغافورة، لكن التقرير الأخير الصادر من الوكالة المذكورة في ١٠ فبراير، ٢٠٢٠ لم يُصدر أمر بسحب الدواء من الأسواق الأمريكية، ربما لأن الفحوصات لم تبين وجود نسبة تتعدى المعدل المقبول من المادة في الدواء، أو ربما لرغبة الوكالة في التأني وعدم التسرع في الإقدام على عملية سحب لدواء مهم ومحوري يستخدمه ملايين الناس لسبب قد لايكون ضرورياً ، والتسبب في أزمة كبرى تكون أضرارها أكبر من فوائدها المحتملة.
ينبغي التنويه أن عملية سحب الأدوية هو إجراء احترازي وقائي وليس لأن الدواء قد تسبب في ضرر ما للمرضى.
في الختام أجد لزاماً أن أؤكد على هذه التوصية المهمة التي ينبغي حفظها والعمل بها: أنه في حال الإعلان عن سحب أي دواء، لا ينبغي التوقف عن استعمال الدواء فوراً، بل يجب البقاء على استخدام الدواء، والتواصل مع الطبيب المختص في أقرب فرصة وأخذ نصيحته في استخدام دواء بديل.
النص المترجم:
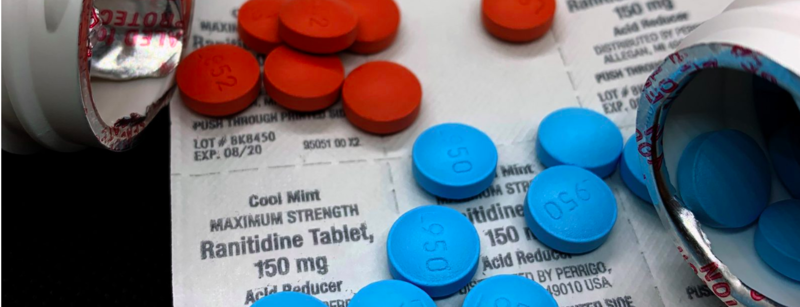
أدوية فالسارتان Valsartan، و رانيتيدين ranitidine، وميتفورمين metformin. هذه الأدوية منتشرة في كل مكان ، ومعتمدة من قبل إدارة الغذاء والدواء الأمريكية (FDA) وموجودة في السوق منذ سنوات والتي يفترض المستهلكون أنها آمنة ضمن قيودها المعروفة. لكن منذ عامين ، وصناعة الأدوية تستنتج بأن الأمور ليست كذلك.
المادة المسببة للسرطان المشتبه بها وهي N- نيتروسو ثنائي ميثيل أمين N-nitrosodimethylamine وتختصر ب NDMA قد ظهرت هذه المادة لأول مرة (2) في داوء فالسارتان ثم في داوء رانيتيدين وفي مذيب دايمثيل فورما أميد DFM، وهو مذيب شائع يستخدم في جميع جوانب الصناعة. إدارة الغذاء والدواء تختبر الآن الميتفورمين لذلك الغرض أيضًا. تقر إدارة الغذاء والدواء (FDA) أنه ومن خلال الاختبارات الجديدة الأكثر تطوراً، فإن [هذه المادة المسرطنة] تمثل مشكلة ستستمر في الظهور في صناعة الأدوية في المستقبل المنظور، مما يخلق حالة ريب للمستهلكين والصناعة على حد سواء.
اكتشاف مادة NDMA المسرطنة، أحيانًاً ذات صلة بالتصنيع، قد أدت إلى إلغاء / استرجاع مئات الآلاف من زجاجات الأدوية ، مما جعل هذا الاسترجاع يتسبب في هدر في التكاليف والوقت.
وبينما أكدت إدارة الغذاء والدواء للمستهلكين أن خطر الإصابة بالسرطان الناجم عن شوائب في أدويتهم أقل من خطر التخلي /التوقف عنها، إلا أن التهديد الجديد ترك الكثيرمن الناس قلقين . والمشكلة تبدو أنها تزداد سوءًا وليس في طريقها للتحسن.
“أنا واثق من أنه ستظل هناك مشاكل في المستقبل القريب في المنتجات الدوائية، ومدى مشاكل الأدوية التي نتأمل فيها، خاصة الزانتاك Zantac (رانيتيدين ranitidine)، غير معروفة بعد. يقول ديفيد لايت، المؤسس والرئيس التنفيذي لشركة ڤاليسور Valisure، وهي صيدلية على الإنترنت مرتبطة بشركة متطورة لفحص الأدوية، إن وجهة نظرنا هي أنها مشكلة خطيرة حقًا.
لايتLight، وشريكه وصديق من جامعة ييل، آدم كلارك-جوزيف ،انتهوا الى لبّ المشكلة بعد الفحص الذي أجرته ڤاليسور Valisure أن كل دفعة تبيعها تظهر مادة NDMA في الرانيتيدين، وهو المكون الفعال في أدوية حمض المعدة الشهيرة مثل الزانتاك Zantac.
كما رفعت شركة ڤاليسور التي مقرها نيو هافين في ولاية كونيتيكت عريضة ( عريضة توفرها هيئة الغذاء والدواء FDA للمواطنين والهيئات لتقديم التماس لـ FDA لتغيير سياسة صحية معينة، معلومات أكثر في 4 ) قائلة إن إدارة الغذاء والدواء الأمريكية تحتاج إلى التحقيق في المذيب المستخدم غالبًا في صناعة الأدوية، DMF، لأنه يصنف على أنه مادة مسرطنة من الفئة الثانية.
وتؤكد صيدلية فڤاليسور أن استخدام مذيب الـ DMF هو المسؤول عن الكثير من مادة الـ NDMA الموجودة في سلسلة توريد الأدوية. تقول عريضة الالتماس إن إدارة الغذاء والدواء الأمريكية يجب أن تخفض المستوى المقبول من استخدام الـ DMF في إمدادات الأدوية الأمريكية وتطلب من الـ FDA أو تسعى إلى استرجاع /إلغاء جميع الأدوية آلتي يوجد فيها الـ DMF بمستويات تزيد عن التوجيهات الإرشادية.
هيئة الغذاء والدواء الأمريكية، التي كانت في البداية غافلة عن مشكلة الـ NDMA، أشارت في بيان أرسل عبر البريد الإلكتروني إلى أنها تواصل اختبارالأدوية التي يزيد تصنيعها من خطر تكوّن شوائب النيتروس أمين nitrosamine، بما في ذلك الـ ARBs ، وهي الرانيتيدين والميتفورمين. الهيئة تقول أنها سوف تنظر أعمق لو ظهرت قضايا جديدة وستطلب من مصنعي الأدوية فحصها لمحتواها من الشوائب أولشوائب غير معروفة في أدوية أخرى، كما يمليه العلم.
أحد الأسباب هو أن المشكلة اكتشفت في غضون العامين الأخيرين، تقول الـ FDA ، أن الطرق التحليلية الجيدة يمكنها اكتشاف كميات ضئيلة من الشوائب، عوامل الخطر هذه يمكن أن تكتشف وتخفف، ولكن لا يمكن عملها جميعاً بين ليلة وضحاها، كما تقول الهيئة.
تحذيرات الهيئة معتمدة على أدلة، وجمع المعلومات / البيانات يأخذ وقتاَ وسنواصل العمل للتأكد من أن هذه الأنواع من الشوائب لا تتجاوز الحدود المقبولة حتي يتمكن المرضى من مواصلة تناول أدويتهم بدون قلق/خوف.
يوافق لايت على أن نظام الـ FDA صالح لأكثر الأدوية. أكثر الأدوية آلتي يجري اختبارها للصيدلية هي صالحة. ولكن الأدوية التجارية تشكل أكثر من ٩٠٪ من الأدوية الموصوفة للمرضى في الولايات المتحدة، والعديد منها معتَمد منذ سنوات، فإنه يعتقد أن هذه الصناعة يجب أن تفعّل اختبارات أعمق على كل الأدوية التي تصنعها. وفي هذه الأثناء، يقول، يجب أن يجرى إصلاح نظام المراقبة.
في حين أن هيئة الغذاء والدواء لا تعتمد في بعض الأحيان شركة ڤاليسور valisure كمختبر جهة خارجية مستقل، يقول لايت هذا هو بالضبط المشكلة. “علينا أن نعترف أن هناك مشكلة. وقال لا يمكننا أن نبقي نقول كل ما قد سبق اعتماده فهو مضبوط”. “جزء هام من هذا هو أن نقوم بالتعديل، والعمل خارج مصنعي الأدوية فقط وادارة الغذاء والدواء.”








