دراسة: لماذا التجارب السريرية معقدة للغاية ؟
ترجمة: عدنان أحمد الحاجي
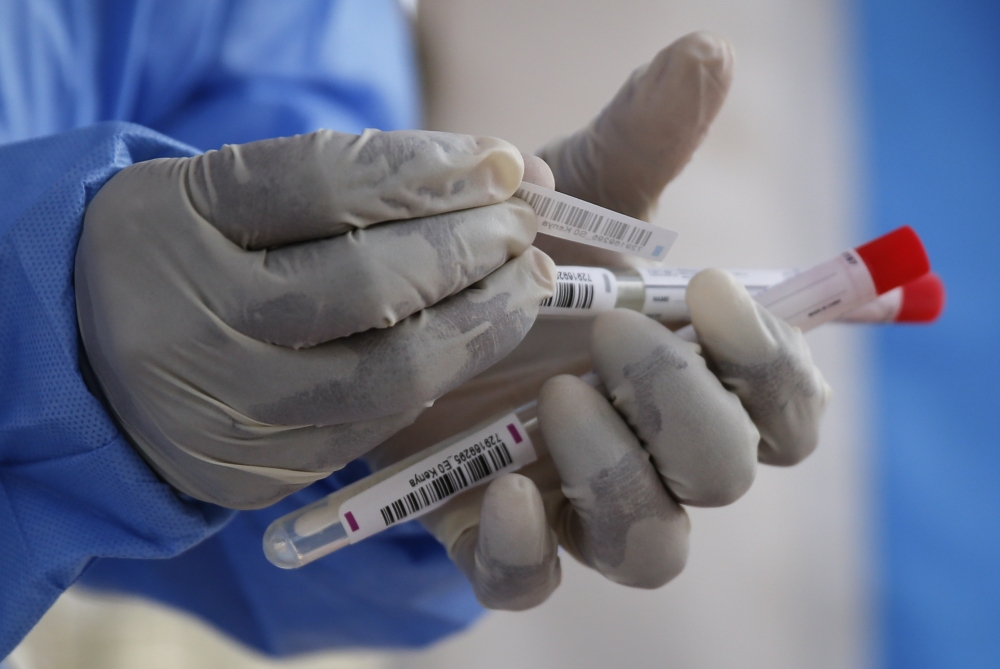
أعلنت وزارة الصحة السعودية بالتعاون مع منظمة الصحة العالمية يوم السبت الموافق ٢ مايو ٢٠٢٠، عن تدشينها لدراسة إكلينيكية موسعة ومتعددة المراكز في سبع مستشفيات حول المملكة.
تهدف الدراسة إلى تجربة فعالية أربع طرق علاج لمعالجة مرضى كوفيد-19 في السعودية، تشتمل الدراسة على الأدوية التالية: هايدروكسكي كلوركين hydroxychloroquine, وريتونياڤير / لابيناڤير ritoniavir/lapinavir, وررمدسڤير remedesivir و إنترفيرون interferon، أثبتت الدراسات المخبرية فعالية أولية لهذه الأدوية، مما تطلب تدشين دراسات إكلينيكية واسعة وجيدة التصميم على المرضى للتأكد من فعاليتها ومأمونيتها (سلامتها).
بدأت المملكة العربية السعودية منذ أعوام، خطوات جادة في الإنشاء المؤسسي لجهات رسمية تعنى بضبط ومراقبة سير عمل الدراسات الإكلينيكية وفق الضوابط العلمية والأخلاقية المتبعة دوليا.
فقامت بإنشاء اللجنة الوطنية للأخلاقيات الحيوية والطبية عام 1992، وكذلك أسندت لهيئة الغذاء والدواء السعودية وضع الشروط والضوابط الخاصة بإجراء الدراسات الإكلينيكية على الأدوية، وقد عملت كلتا الجهتين معا لمنع التداخل بين اختصاصاتهما، وتسهيل العمل على الباحثين، وأثمرت هذه الجهود الوصول إلى أفضل مستوى ممكن من الممارسة الأخلاقية للدراسات الإكلينيكية.
من أجل ضمان حقوق الباحثين والمشاركين والممولين للدراسات، وضمان السرية والخصوصية لكل أطراف الدراسة، وكافة الشؤون الأخلاقية والقانونية والعلمية والاقتصادية ذات العلاقة.
المقال المترجم بين أيدينا (مستقى من مدونة علمية تهتم بأخبار البحوث الدوائية، والكاتب هو باحث كيميائي ومطور للأدوية)، يشير الكاتب في مقاله بجلاء إلى صعوبة، وتعقيد إنشاء وتصميم دراسة إكلينيكية، لما تتطلبه من تمويل مالي ضخم، وتوظيف شركات عدة تعنى بدراسة الجوانب الاقتصادية واللوجستية والعلمية كافة، بما فيها شركات لحساب الكلفة الاقتصادية للدراسة، وشركات توظيف لاستجلاب المشاركين والمتطوعين.
والعمل كذلك على وضع تصميم محكم وعلمي يلبي الاشتراطات الصارمة والدقيقة، لمجموعة الخبراء والباحثين المستقلين المراقبين للدراسة.
وما يتطلبه أيضا من تقديم كافة الوثائق والمستندات المطلوبة (التي قد تصل المئات عن كل شيء يتعلق بالدراسة بالتفصيل)، للهيئة الرسمية الممثلة في هيئة الغذاء والدواء السعودية، بحيث يقوم الخبراء المستقلون بالمراقبة والإشراف على سير جميع مراحل الدراسة ومراقبتها.
مراقبة مكثفة للتأكد من مسيرتها وفق البوتوكولات الموضوعة والشروط واللوائح الناظمة لها، وبعد ذلك يأتي دور خبراء مستقلين آخرين للنظر في نتائج الدراسة وتدقيقها ونقدها.
وتوجيه الكثير من الاستفسارات والإستيضاحات إلى الباحثين القائمين على الدراسة لكي يجيبوا عنها، وبعد موافقة هذه اللجنة المحكِّمة للدراسة وإجازتها لها، تحوز على الموافقة بالنشر، وبعد ذلك ترفع الشركة أو المؤسسة أوراقها لهيئة الغذاء والدواء السعودية للاعتماد النهائي.
هذه الرحلة الطويلة تشرح سبب طول أمد الدراسات الإكلينيكية وصعوبة إجراءتها وارتفاع تكلفتها، فبعد المرور عبر كل هذه الخطوات الشاقة والمضنية جدا.
قد يحصل الدواء بعدها على الاعتماد النهائي ويسمح بنزوله للأسواق، وقد يفشل في أي مرحلة من مراحلها وتخسر الشركة الملايين، قد يتساءل البعض؛ لماذا كل هذا التعقيد والإصرار على الإغراق في التفاصيل الدقيقة، والتي تستهلك الكثير من الوقت والجهد، لماذا لا يصار إلى تسريع وتبسيط الدراسات ونحن في أتون جائحة ونحتاج إلى حل سريع ولا نملك رفاهية الوقت والانتظار؟
الجواب: أن هذه الطريقة المحددة للدراسات الاكلينيكية، هي ما اتفق عليها المجتمع العلمي ووجد فيها الضمانة الأخلاقية والعلمية من الوقوع في فخ الانحياز والخطأ والوهم.
والحصول على أفضل نتيجة ممكنة أخلاقيا وعلميا، خير ختام للكلام (مقولة شائعة) بين الباحثين والقائمين على الدراسات، تعطي إشارة واضحة على أهمية الدقة والصرامة فيها: “جميع القواعد والضوابط المذكورة أعلاه بُنيت و صُممت في الواقع على أسرّة المستشفيات وحول المقابر”
يبدو، من الخارج، كما يحدث في أكثر الأوقات وكنفقات التجارب السريرية أن المسألة في الواقع هي مجرد بيروقراطية.
يمكنني بسهولة آخذ في الإعتبار العديد من المركبات الكيميائية (بعضها معتمد من قبل هيئة الغذاء والدواءFDA ولكنها لم تعد تصنع الآن، وبعضها أعتمد من دول خارج الولايات المتحدة، وبعضها موجود بشكل طبيعي ويباع كمكملات) مما يمكنني حرفيا إجراء تجربة عليها في شقتي،
لو كان السؤال الوحيد هو ” هل هذايعمل فعلا؟ “.
التركيب الكيميائي سهل بما فيه الكفاية مما يمكنك عمله به حتى في مطبخك، خطوة أو خطوتين بمعدات بسيطة ومواد شائعة تستخدم في التفاعل.
لدى أصدقائي أجهزة تحليليلية من بينها غروماتوكرغافيا السوائل الموصلة بمطياف الكتلة LC / MS والرنين المغناطيسي النووي NMR متاحة للاستخدام، أو إذا لم يكن ذلك ممكنا، فهناك مختبرات تحليلية قمت بإرسال عينات إليها بتكلفة قدرها بضع مئات من الدولارات.
انتاج الدواء الوهمي أمر سهل، حتى أن غورين Gwern لديه بروتوكول لإجراء تجربة مقارنة بإعطاء دواء لمجموعة من المرضى وإعطاء دواء وهمي لمجموعة أخرى على نفسك.
على الرغم من أن ذلك لن يكون ضروريا لو أرسلت للناس المركب الكيميائي (أو الدواء الوهمي) بالبريد وقمت بالتعشية randomization في المنزل، وهناك بالفعل دراسات تفحص آثار الأدوية ، وتجمع المعلومات من المشاركين ، وما إلى ذلك، بالكامل عبر الإنترنت ببعض البرامج البسيطة جدا- نظرا لأن أدوية الهلوسة، ما زالت تحت المراقبة، في هذه الحالة المشاركون مجهولون تماما.
الآن، من المسلم به، ان القيام بذلك بهذه الميزانية المنخفضة يدور الكثير من الزوايا.
وأنا متأكد من أن البيانات من شأنها أن تكون أكثر صخبا مما ستكون عليه في تجربة المرحلة الثانية التقليدية، لذلك ستحتاج إلى حجم عينة أكبر، وتركيب الكثير من الأدوية صعب، ولا يمكن حقن أدوية مثل سبينرازا Spinraza ذاتيا [دواء يستخدم في علاج ضمور العضلات الشوكي ويحقن حول الحبل الشوكي ]، وما إلى ذلك، مما يضيف المزيد من التعقيد.
ولكن على الرغم من ذلك، لا يبدو هذا بالفعل أنه ينبغي أن يتطلب 100 مليون دولار، وفريق من المحامين، وشركة من شركات الضغط وغوانشي خاصة guanxi [كلمة من أصل صيني تعني شبكة من الوساطات/ الواسطة].
لكل تجربة تقوم بها، هل أنا مخطيء تماما هنا؟، حسنا، يمكنني أن أرى أن بعض هذا الاستعلام قادم من حركة الاختراق البيلوجيbiohacking، و يمكن أن أتصور ذلك من ذلك المنظور، اساليب التجارب السريرية لصناعة الأدوية تبدو أنها حبكة معقدة، ومكلفة بلا داع موجب.
ولكن اسمعوني: هناك أسباب لعملها بتلك الطريقة التي نعملها بها، بعض هذه الأسباب أفضل من غيرها، أنا متأكد، إلا أن الأسباب الوجيهة هي في الواقع جيدة حقا.
سأتناول هذه الاقتراحات بنفس الترتيب التي وردت به في رسالة البريد الإلكتروني، و اسمحوا لي أن أقول قبل كل شيء أنني لا أحاول أن أسخر من هذه الأفكار، ولا أحاول أقلل من شأن فكرة طرح هذه الأسئلة- إنها أسئلة في محلها وتستحق إجابات جيدة، وتفكيري هو أن تناول هذا المعنى هنا في هذه المدونة، قد يكون ضمن اهتمام الآخرين.
أولا، الجزء عن “التركيب الكيميائي سهل بما فيه الكفاية مما يمكن أن يعمل في مطبخك الخاص”.
هناك في الواقع بعض الأدوية الكثيرة،حيث المكونات الصيدلانية الفعالة يمكن، في الواقع، أن يتم إنتاجها بهذه الطريقة، ولكن دواء ريمدسڤير remdesivir(لاختيار واحد منها وهذا ماهو مسلط عليه الضوء الآن) ليست واحد من تلك الأدوية.
في تجربة المعاهد الوطنية للصحة/ والمعهد الوطني للحساسية والامراض المعدية NIAID التي بدأت بنشر التقرير عن 286 شخصا عولجوا بريمدسڤير.
حيث أعطوا 200 مغ في اليوم الأول و 100مغ في اليوم الذي بعده لمدة عشرة أيام، دعونا نقول بمعدل 7 أيام- لذلك العدد من المرضى كنا بحاجة إلى ما يزيد قليلا على 228 غراما من ريمدسڤير remdesivir لتلبية الكمية المحددة.
كم تحتاج منه للقيام بالتجربة السريرية؟ حسنا، هناك شركات قائمة بذاتها لمساعدتك على حساب كم تحتاج منه في التجارب السريرية.
-لو نفد الدواء اثناء التجربة السريرية، فتصبح التجربة كلها في مهب الريح، وإذا أنتجت منه فوق الحاجة فأنت تبذر المال، مجرد وجود مثل هذه الأعمال التجارية المتخصصة هو موضوع يدعو إلى التأمل، ولكن لو أن الدواء بدا وكأنه ينفد من عندك، ألا يمكنك فقط انتاج المزيد منه؟ وهذا يثير مشكلة كبيرة أخرى: الممارسات المخبرية الجيدة GLP والممارسات الصناعية الجيدة CGMP الحالية.
هاتان الممارستان متشابهتان إلى حد كبير، ولكن لهما متطلبات مختلفة ويتم استخدامهما لأغراض مختلفة.
GLP / CGMP بالفعل تضيفان بيروقراطية الى البيروقراطية الموجودة، لأنهما تضيفان الكثير من الإجراءات الموحدة وأطنانا من الوثائق المطلوبة، لم أعمل أبدا وفقا لهذه المعايير (أقوم بأبحاث المراحل الأولية، لا ما يصل الى مستوى المرحلة السريرية)، ولن أستمتع بذلك، من المؤكد أنه سيجعل الأمور تتحرك بشكل أسرع للتخلص من الأشياء.
لكن هذه فكرة سيئة، لا يمكنك أن تلفق الأمور عندما تعطي دواءا للناس، خارج المشاكل الأخلاقية المطلقة ل “اتكل، وخذ الدواء.
ربما يكون جيدا بما يكفي لأمثالك”، هناك حاجة للتأكد من أن كل شيء موحد تماما بحيث تكون بياناتك السريرية نفسها فرصة أفضل لتعني شيئا مفيدا، كمية الضوضاء في البيانات السريرية البشرية تتحدى الاعتقاد إذا لم تكن قد رأيتها شخصيا، يجب أن يكون كل جزء من العملية يمكن تسويته، لأن الأجزاء التي لا يمكنك تسويتها ستقضي تماما على مشروع تطوير الدواء إذا لم تفعل ذلك.
فكرة ال GMP هي التخلص من جميع المخاطر والتباينات التي يمكن التخلص منها عن طريق الفحص، وتوحيد المعايير – وما تبقى، بشكل مثالي، هو المخاطرة باختبار الدواء نفسه والله أعلم اذا ما ذلك كان كافيا.
حسنا، الآن إذا كان لديك الدواء جاهزا، فقد حان الوقت لإستجلاب مرضى لتجربة الدواء عليهم، حسنا، في الواقع، فقد حان الوقت لتصميم التجربة قبل البدء في استجلاب مرضى لإجراء التجربة، وهذا مجال كامل في حد ذاته، قد تتصور أن دراسة دواء واحد في بيئة مرضية معدية قد يكون أحد تصميمات التجارب الأكثر بساطة، وهذا صحيح في الواقع، ولكن هذا بسيط فقط على المستوى النسبي.
أولا، ما هي نقاطك النهائية، ما الذي ستقوم بقياسه لمعرفة ما إذا كان الدواء يعمل؟
في حالة تجربة فيروس كورونا، هل تريد قياس الحمل الفيروسي، ووظيفة الرئة، وحدة المرض بشكل عام، وعدد الأيام قبل ان يسمح للمريض بمغادرة المستشفى، وعدد الأيام قبل أن يموت المريض؟ ربما كل هذه الأمور، بالتأكيد، ولكن أي منها تعتبره أنه نقطة النهاية الأكثر أهمية (الأولية)، النقطة التي تهدف بقية قراراتك المتعلقة بتصميم التجربة السريرية للإجابة عليها؟الآن، لتلك القرارات.
كم عدد الجرعات التي ستجربها على المريض؟ كيف تعرف أنك اخترت عدد الحرعات الأكثر فائدة؟ ماهي أنواع المرضى الذين ستقوم باستجلابهم للتجربة؟
في هذه الحالة، لديك العديد من المتغيرات المعروفة التي يجب مراعاتها (أو أن تضعها جانبا، إذا كان بإمكانك ان تبرر ذلك أيضا): شدة المرض، والوقت منذ بداية الأعراض، والعمر والجنس ووزن الجسم والأدوية الأخرى التي يتناولها المريض، والأمراض المصاحبة المعروفة التي يعاني منها كارتفاع ضغط الدم، وهلم جرا.
أثناء تسجيل المرضى، ستحتاج إلى التحكم في أكبر عدد ممكن من هذه المتغيرات وموازنتها قدر الإمكان في كل ذراع من الدراسة.
كم عدد أدرعة الدراسة التي ستتناولها ؟ كم عدد المرضى الذين تعتقد أنك ستحتاجهم لكل ذراع، حتى تكون النتائج ذات معنى؟ أين ستجدهم؟ من سيفحص ويجمع كل البيانات الأولية، ومن سيتابع كل عملية من عمليات جمع البيانات أثناء التجربة؟. حتى دراسة المرحلة الأولية (الأفراد العاديون، الذين لا يعانون من أي مرض، ومعظمهم يفحصون مستويات الدم، ويبحثون عن أي إشارات أمان ظاهرية)، يتعين عليها اختيار أعضائها بعناية للتأكد من أن كل شيئ يمضي بسلاسة في المرحلة الثانية.
وبما أنك تتحدث عن تجربة “هل هذا يعمل فعلا”، فهذه هي المرحلة الثانية بحسب التعريف.
إن إرسال الدواء للمشاركين عبر البريد ومطالبتهم بتناوله سيضيف الكثير من التشتت (التفرق) غير الضروري إلى البيانات، لأن بعض الأشخاص سينسون أن يتناولوا الدواء، وسيحاول البعض من هؤلاء مضاعفة الكمية في اليوم التالي، وبعضهم غير متأكد مما إذا كانوا قد تناولوا الجرعة بالأمس أم لم يتناولوها.
البعض منهم قد تناول الدواء، والبعض الآخر لم يتناوله، والبعض الآخر قد يتذكر فجأة أثناء ذهابهم الي فراش النوم.
كلما زاد عدد الأشخاص المشاركين في التجربة، كلما زاد عدد هؤلاء الناس من هذا النوع، ومن المرجح أن تتماشى تلك المشاكل بالتوازي، مع أي ميزة من مميزات حجم العينة الكبيرة ولذلك تلغي فائدة تلك الميزة مباشرة، أنا لا أختلق هذا: اسأل أي طبيب للتحدث بصراحة عن امتثال المرضى للتوصيات، واستعد للسماع منه ما يملأ سمعك من الكلام.
حتى أشياء مثل تناول الدواء أثناء وجبة الإفطار مع عصير البرتقال، مقابل تناولها مع عصير الغريب فروت، يمكن أن يحدث فرقا كبيرا (وهو شيء بقي غير مدرك لسنوات).
لكننا نتحدث عن المرحلة الثانية، لذلك قد يكون هؤلاء المرضى مرضى جدا ، أو حتى مرضى المستشفى بدوام كامل (كما هو الحال في حالات فيروس كورونا)، لذا فأنت تتحدث تلقائيا مع أطباء وممرضين، وما إلى ذلك، وعليك معرفة أين ستجد مثل هؤلاء الأشخاص المستعدين لإضافة عبء مساعدتك في تجربتك السريرية إلى واجباتهم اليومية. ؟ من الذي يتابع كل هؤلاء الأشخاص ويتأكد من أن سجلات ملاحظاتهم تجري كما ينبغي؟
لأسباب أخلاقية وعملية، تحتاج أيضا إلى مجموعة أخرى من الأشخاص يراقبون كل شيء.
هؤلاء الأشخاص، يسمون بلجنة المراقبة، هم الإجابة على السؤال القديم الخاص: “من سيحرس الحراس”، وسوف يكونون في جانب القضية بأكملها، مفوضين للنظر في البيانات التي يتم إنشاؤها في نقاط محددة أثناء التجربة للتأكد، أن الأمور تسير كما خطط لها.
معظم الوقت سيقولون “استمر”، لكن عدد معقول من التجارب سينتهي لأن المراقبين قالوا”ليس لديك فرصة لاستيفاء متطلبات نقاطك النهائية – توقف الآن.
إنه غير مجد وغير أخلاقي أن تستمر في إعطائك الناس دواءك”، من حين لآخر، وقد يقولون “توقف الآن- دواؤك جيد جدا لدرجة أنه من غير الأخلاقي عدم إعطائه للجميع في التجربة السريرية “، ولكن تمر سنوات حين لا يحدث ذلك، في أي شيء في الصناعة، في كلتا الحالتين، تحتاج إلى بعض الخبراء من خارج التجربة الذين لا يشاركون في الجرعات والأجزاء اليومية من التجربة ، والذين ليسوا جزءا من مجموعة لها مصلحة مثبتة في النتائج.
هؤلاء هم الأشخاص الذين اخرجوا مدير تنفيذي كبير لشركة بفليزرPfizerمن استحمامه صباح يوم أحد.
لإخباره أن مراجعة البيانات أظهرت أن أكبر مشروع لتطوير الأدوية، للشركة على الإطلاق (برنامج القلب والأوعية الدموية لرفع مستوي الكلسترول النافع HDL) كان بالتأكيد (و بشكل غير متوقع)، قد قتل مجموعة العلاج بمعدل أعلى قليلا من مجموعة التحكم، في تجربة المرحلة الثالثة التي تضم عدة آلاف من المرضى، وهو نوع الأشياء التي تريد معرفتها من أول فرصة.
إن الصعوبة الكبرى في إدارة تجربة على البشر بالطريقة التي تقترحها، على الرغم من ذلك، هي أنك ستفتح نفسك على ملاحقة جنائية حين تقوم بذلك.
تريد هيئة الغذاء والدواء الأمريكية أن تسمع عن دوائك قبل إعطائه للبشر: ما هي ماهيته، وماذا تتوقع منه أن يفعل ولماذا، وتفاصيل (GMP!) عن كيف انتجته، وما مدي ما أنت متأكد من أنك قمت بإنتاج ما تعتقد أنك قد أنتجته، ما هو تصميم تجربتك السريرية، ولماذا اخترت ذلك التصميم، وما الذي ستبحث عنه أثناء القيام بتنفيذها.
هذا يسمى بالتطبيق الدوائي الجديد الاستقصائي IND، وهو أمر مؤذ ومقرف، في ظل الظروف الوبائية.
تعمل الهيئة بالفعل على تسريع هذا النوع من الأشياء وتدوير الزوايا، لكنها لا تسقطها لنفس الأسباب التي لا تؤدي فقط إلى إسقاط CGMP، مرة أخرى، يمكننا أن نتجادل حول ما إذا كانت الخلفية المناسبة، هي البدء في اعطاء جرعات دواء استقصائي للأشخاص المشاركين في التجربة.
وما هي العقوبات التي يجب أن تقرر لو قررت تجاهلها- ولكن هذه هي التفاصيل والدرجات.
سألتزم بشدة بموقفي أنك تحتاج إلى نوع من بيان مكتوب، وخطة وأساس منطقي ووثائق، التي عليك أن تعملها بشكل صحيح، ولكن يجب مراجعتها من قبل فريق خارجي يعرف العمل بشكل جيد ولكن ليس من ضمن العمل التجاري، وهذا هو ما تقوم به هيئة الغذاء والدواء
في تجربة المعاهد الوطنية للصحة/ والمعهد الوطني للحساسية والامراض المعدية NIAID التي بدأت بنشر التقرير عن 286 شخصا عولجوا بريمدسڤير.
حيث أعطوا 200 مغ في اليوم الأول و 100مغ في اليوم الذي بعده لمدة عشرة أيام، دعونا نقول بمعدل 7 أيام- لذلك العدد من المرضى كنا بحاجة إلى ما يزيد قليلا على 228 غراما من ريمدسڤير remdesivir لتلبية الكمية المحددة.
كم تحتاج منه للقيام بالتجربة السريرية؟ حسنا، هناك شركات قائمة بذاتها لمساعدتك على حساب كم تحتاج منه في التجارب السريرية.
-لو نفد الدواء اثناء التجربة السريرية، فتصبح التجربة كلها في مهب الريح، وإذا أنتجت منه فوق الحاجة فأنت تبذر المال، مجرد وجود مثل هذه الأعمال التجارية المتخصصة هو موضوع يدعو إلى التأمل، ولكن لو أن الدواء بدا وكأنه ينفد من عندك، ألا يمكنك فقط انتاج المزيد منه؟ وهذا يثير مشكلة كبيرة أخرى: الممارسات المخبرية الجيدة GLP والممارسات الصناعية الجيدة CGMP الحالية.
هاتان الممارستان متشابهتان إلى حد كبير، ولكن لهما متطلبات مختلفة ويتم استخدامهما لأغراض مختلفة.
GLP / CGMP بالفعل تضيفان بيروقراطية الى البيروقراطية الموجودة، لأنهما تضيفان الكثير من الإجراءات الموحدة وأطنانا من الوثائق المطلوبة، لم أعمل أبدا وفقا لهذه المعايير (أقوم بأبحاث المراحل الأولية، لا ما يصل الى مستوى المرحلة السريرية)، ولن أستمتع بذلك، من المؤكد أنه سيجعل الأمور تتحرك بشكل أسرع للتخلص من الأشياء.
لكن هذه فكرة سيئة، لا يمكنك أن تلفق الأمور عندما تعطي دواءا للناس، خارج المشاكل الأخلاقية المطلقة ل “اتكل، وخذ الدواء.
ربما يكون جيدا بما يكفي لأمثالك”، هناك حاجة للتأكد من أن كل شيء موحد تماما بحيث تكون بياناتك السريرية نفسها فرصة أفضل لتعني شيئا مفيدا، كمية الضوضاء في البيانات السريرية البشرية تتحدى الاعتقاد إذا لم تكن قد رأيتها شخصيا، يجب أن يكون كل جزء من العملية يمكن تسويته، لأن الأجزاء التي لا يمكنك تسويتها ستقضي تماما على مشروع تطوير الدواء إذا لم تفعل ذلك.
فكرة ال GMP هي التخلص من جميع المخاطر والتباينات التي يمكن التخلص منها عن طريق الفحص، وتوحيد المعايير – وما تبقى، بشكل مثالي، هو المخاطرة باختبار الدواء نفسه والله أعلم اذا ما ذلك كان كافيا.
حسنا، الآن إذا كان لديك الدواء جاهزا، فقد حان الوقت لإستجلاب مرضى لتجربة الدواء عليهم، حسنا، في الواقع، فقد حان الوقت لتصميم التجربة قبل البدء في استجلاب مرضى لإجراء التجربة، وهذا مجال كامل في حد ذاته، قد تتصور أن دراسة دواء واحد في بيئة مرضية معدية قد يكون أحد تصميمات التجارب الأكثر بساطة، وهذا صحيح في الواقع، ولكن هذا بسيط فقط على المستوى النسبي.
أولا، ما هي نقاطك النهائية، ما الذي ستقوم بقياسه لمعرفة ما إذا كان الدواء يعمل؟
في حالة تجربة فيروس كورونا، هل تريد قياس الحمل الفيروسي، ووظيفة الرئة، وحدة المرض بشكل عام، وعدد الأيام قبل ان يسمح للمريض بمغادرة المستشفى، وعدد الأيام قبل أن يموت المريض؟ ربما كل هذه الأمور، بالتأكيد، ولكن أي منها تعتبره أنه نقطة النهاية الأكثر أهمية (الأولية)، النقطة التي تهدف بقية قراراتك المتعلقة بتصميم التجربة السريرية للإجابة عليها؟الآن، لتلك القرارات.
كم عدد الجرعات التي ستجربها على المريض؟ كيف تعرف أنك اخترت عدد الحرعات الأكثر فائدة؟ ماهي أنواع المرضى الذين ستقوم باستجلابهم للتجربة؟
في هذه الحالة، لديك العديد من المتغيرات المعروفة التي يجب مراعاتها (أو أن تضعها جانبا، إذا كان بإمكانك ان تبرر ذلك أيضا): شدة المرض، والوقت منذ بداية الأعراض، والعمر والجنس ووزن الجسم والأدوية الأخرى التي يتناولها المريض، والأمراض المصاحبة المعروفة التي يعاني منها كارتفاع ضغط الدم، وهلم جرا.
أثناء تسجيل المرضى، ستحتاج إلى التحكم في أكبر عدد ممكن من هذه المتغيرات وموازنتها قدر الإمكان في كل ذراع من الدراسة.
كم عدد أدرعة الدراسة التي ستتناولها ؟ كم عدد المرضى الذين تعتقد أنك ستحتاجهم لكل ذراع، حتى تكون النتائج ذات معنى؟ أين ستجدهم؟ من سيفحص ويجمع كل البيانات الأولية، ومن سيتابع كل عملية من عمليات جمع البيانات أثناء التجربة؟. حتى دراسة المرحلة الأولية (الأفراد العاديون، الذين لا يعانون من أي مرض، ومعظمهم يفحصون مستويات الدم، ويبحثون عن أي إشارات أمان ظاهرية)، يتعين عليها اختيار أعضائها بعناية للتأكد من أن كل شيئ يمضي بسلاسة في المرحلة الثانية.
وبما أنك تتحدث عن تجربة “هل هذا يعمل فعلا”، فهذه هي المرحلة الثانية بحسب التعريف.
إن إرسال الدواء للمشاركين عبر البريد ومطالبتهم بتناوله سيضيف الكثير من التشتت (التفرق) غير الضروري إلى البيانات، لأن بعض الأشخاص سينسون أن يتناولوا الدواء، وسيحاول البعض من هؤلاء مضاعفة الكمية في اليوم التالي، وبعضهم غير متأكد مما إذا كانوا قد تناولوا الجرعة بالأمس أم لم يتناولوها.
البعض منهم قد تناول الدواء، والبعض الآخر لم يتناوله، والبعض الآخر قد يتذكر فجأة أثناء ذهابهم الي فراش النوم.
كلما زاد عدد الأشخاص المشاركين في التجربة، كلما زاد عدد هؤلاء الناس من هذا النوع، ومن المرجح أن تتماشى تلك المشاكل بالتوازي، مع أي ميزة من مميزات حجم العينة الكبيرة ولذلك تلغي فائدة تلك الميزة مباشرة، أنا لا أختلق هذا: اسأل أي طبيب للتحدث بصراحة عن امتثال المرضى للتوصيات، واستعد للسماع منه ما يملأ سمعك من الكلام.
حتى أشياء مثل تناول الدواء أثناء وجبة الإفطار مع عصير البرتقال، مقابل تناولها مع عصير الغريب فروت، يمكن أن يحدث فرقا كبيرا (وهو شيء بقي غير مدرك لسنوات).
لكننا نتحدث عن المرحلة الثانية، لذلك قد يكون هؤلاء المرضى مرضى جدا ، أو حتى مرضى المستشفى بدوام كامل (كما هو الحال في حالات فيروس كورونا)، لذا فأنت تتحدث تلقائيا مع أطباء وممرضين، وما إلى ذلك، وعليك معرفة أين ستجد مثل هؤلاء الأشخاص المستعدين لإضافة عبء مساعدتك في تجربتك السريرية إلى واجباتهم اليومية. ؟ من الذي يتابع كل هؤلاء الأشخاص ويتأكد من أن سجلات ملاحظاتهم تجري كما ينبغي؟
لأسباب أخلاقية وعملية، تحتاج أيضا إلى مجموعة أخرى من الأشخاص يراقبون كل شيء.
هؤلاء الأشخاص، يسمون بلجنة المراقبة، هم الإجابة على السؤال القديم الخاص: “من سيحرس الحراس”، وسوف يكونون في جانب القضية بأكملها، مفوضين للنظر في البيانات التي يتم إنشاؤها في نقاط محددة أثناء التجربة للتأكد، أن الأمور تسير كما خطط لها.
معظم الوقت سيقولون “استمر”، لكن عدد معقول من التجارب سينتهي لأن المراقبين قالوا”ليس لديك فرصة لاستيفاء متطلبات نقاطك النهائية – توقف الآن.
إنه غير مجد وغير أخلاقي أن تستمر في إعطائك الناس دواءك”، من حين لآخر، وقد يقولون “توقف الآن- دواؤك جيد جدا لدرجة أنه من غير الأخلاقي عدم إعطائه للجميع في التجربة السريرية “، ولكن تمر سنوات حين لا يحدث ذلك، في أي شيء في الصناعة، في كلتا الحالتين، تحتاج إلى بعض الخبراء من خارج التجربة الذين لا يشاركون في الجرعات والأجزاء اليومية من التجربة ، والذين ليسوا جزءا من مجموعة لها مصلحة مثبتة في النتائج.
هؤلاء هم الأشخاص الذين اخرجوا مدير تنفيذي كبير لشركة بفليزرPfizerمن استحمامه صباح يوم أحد.
لإخباره أن مراجعة البيانات أظهرت أن أكبر مشروع لتطوير الأدوية، للشركة على الإطلاق (برنامج القلب والأوعية الدموية لرفع مستوي الكلسترول النافع HDL) كان بالتأكيد (و بشكل غير متوقع)، قد قتل مجموعة العلاج بمعدل أعلى قليلا من مجموعة التحكم، في تجربة المرحلة الثالثة التي تضم عدة آلاف من المرضى، وهو نوع الأشياء التي تريد معرفتها من أول فرصة.
إن الصعوبة الكبرى في إدارة تجربة على البشر بالطريقة التي تقترحها، على الرغم من ذلك، هي أنك ستفتح نفسك على ملاحقة جنائية حين تقوم بذلك.
تريد هيئة الغذاء والدواء الأمريكية أن تسمع عن دوائك قبل إعطائه للبشر: ما هي ماهيته، وماذا تتوقع منه أن يفعل ولماذا، وتفاصيل (GMP!) عن كيف انتجته، وما مدي ما أنت متأكد من أنك قمت بإنتاج ما تعتقد أنك قد أنتجته، ما هو تصميم تجربتك السريرية، ولماذا اخترت ذلك التصميم، وما الذي ستبحث عنه أثناء القيام بتنفيذها.
هذا يسمى بالتطبيق الدوائي الجديد الاستقصائي IND، وهو أمر مؤذ ومقرف، في ظل الظروف الوبائية.
تعمل الهيئة بالفعل على تسريع هذا النوع من الأشياء وتدوير الزوايا، لكنها لا تسقطها لنفس الأسباب التي لا تؤدي فقط إلى إسقاط CGMP، مرة أخرى، يمكننا أن نتجادل حول ما إذا كانت الخلفية المناسبة، هي البدء في اعطاء جرعات دواء استقصائي للأشخاص المشاركين في التجربة.
وما هي العقوبات التي يجب أن تقرر لو قررت تجاهلها- ولكن هذه هي التفاصيل والدرجات.
سألتزم بشدة بموقفي أنك تحتاج إلى نوع من بيان مكتوب، وخطة وأساس منطقي ووثائق، التي عليك أن تعملها بشكل صحيح، ولكن يجب مراجعتها من قبل فريق خارجي يعرف العمل بشكل جيد ولكن ليس من ضمن العمل التجاري، وهذا هو ما تقوم به هيئة الغذاء والدواء.






